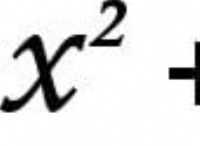チオ硫酸塩とヨウ素の間の反応は、次の方程式で表すことができます。
2S2O3^2- + I2→S4O6^2- + 2i^ -
滴定のエンドポイントでは、チオ硫酸塩のすべてがヨウ素と反応しているため、溶液中にS2O3^2-イオンはもうありません。これは、追加された追加のヨウ素がチオ硫酸塩と反応せず、代わりにI2分子として溶液にとどまることを意味します。これらのI2分子は、可視スペクトルの光を吸収し、溶液に青色を与えます。
三ヨードイオンの形成は、次の方程式で表すことができます。
i2 + i-→i3^ -
i3イオンは、溶液の青色の色にも責任があります。