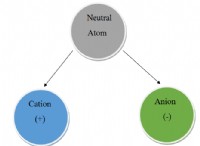
イオン化合物では、ある原子から別の原子への電子の完全な伝達があり、イオンの形成が生じます。積極的に帯電したイオンと負の帯電イオンの間の静電引力は、化合物を一緒に保持します。
共有結合が含まれていない化合物は次のとおりです
- \(\ text {o} _2 \):2つの酸素原子が電子を共有して二重結合を形成するため、これは共有化合物です。
- \(\ text {licl} \):これは、リチウム原子がその原子価電子を塩素原子に伝達し、li+およびcl-イオンの形成をもたらすため、イオン化合物です。
- \(\ text {so} _2 \):硫黄原子が2つの酸素原子と電子を共有して2つの二重結合を形成するため、これは共有化合物です。
したがって、共有結合を含まない化合物は\(\ text {hl} \)および\(\ text {cbr} _4 \)です。