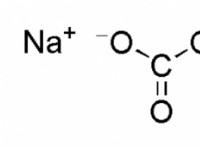
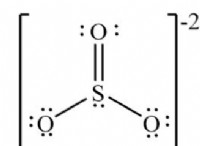
ベースの強度は、水酸化物イオンを寄付する能力によって決定されます。塩基がより多くの水酸化物イオンを寄付できるほど、それは強くなります。いくつかの一般的な複合ベースには以下が含まれます。
*水酸化ナトリウム(NAOH)
*水酸化カリウム(KOH)
*水酸化カルシウム(CA(OH)2)
*水酸化アンモニウム(NH4OH)
これらの塩基はすべて強い塩基です。つまり、水中で完全に解離して水酸化物イオンが放出されます。
一方、弱い塩基は、部分的に水に分離します。一般的な弱い基盤には次のものがあります。
*アンモニア(NH3)
*炭酸(H2CO3)
*酢酸(CH3COOH)
これらの塩基が水に溶解すると、水酸化物イオンが部分的にしか放出されません。これは、それらのpHが強い塩基のpHよりも低いことを意味します。
溶液中の水酸化物イオンの濃度は、pHスケールで測定されます。 pHスケールの範囲は0〜14で、pHは中性です。 7未満のpHは酸性溶液を示し、7を超えるpHは基本的な溶液を示します。
複合ベースは、次のようなさまざまなアプリケーションで重要です。
*クリーニング製品:汚れや汚れを壊す可能性があるため、複合塩基は洗浄製品によく使用されます。
*消臭剤:複合塩基を消臭剤で使用して、汗で生成される酸を中和することができます。
*医薬品:化合物ベースは、制酸剤や下剤を含むさまざまな医薬品で使用されます。
複合ベースは多くの業界にとって不可欠であり、さまざまなアプリケーションで使用されています。