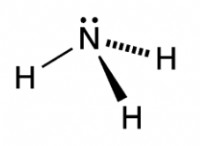
酸素と硫黄はどちらも周期表のグループ16(カルコジェンとも呼ばれます)にあります。同じグループの要素は、同じ数の原子価電子の存在により、同様の化学的性質を共有しています。
酸素と硫黄の両方に6つの価電子があり、安定した電子構成を実現するために2つの電子を獲得する傾向があります。これにより、それらは非常に反応的になり、他の要素と共有結合を形成して外側のシェルを完成させます。
彼らは一般に共有結合に参加して、外側の電子シェルを完成させ、非金属特性を実証します。酸素と硫黄はさまざまな同種形態で存在し、酸素は2つの安定性同位体を持ち、硫黄は4つの安定した同位体を有する。
さらに、酸素と硫黄は、グループを下に移動するにつれて、原子サイズと分子サイズが徐々に増加し、電気陰性度とイオン化エネルギーの低下をもたらします。