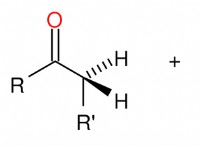
水中の過酸化水素の溶解は、過酸化水素と水分子の極性分子間の分子間相互作用を含む物理的プロセスです。過酸化水素は、酸素と水素原子の間の電気陰性度の違いにより、極性分子です。過酸化水素の酸素原子は部分的な負電荷(Δ-)を持ち、水素原子は部分的な正電荷(Δ+)を持っています。
過酸化水素を水に加えた場合、極水分子は双極子型相互作用を介して極性水素過酸化水素分子と整列し、相互作用します。過酸化水素中の水素原子の部分的な正電荷は、水中の酸素原子の部分的な負電荷に引き付けられ、逆も同様です。これらの分子間相互作用は、水中の過酸化水素の溶解につながります。
水中の過酸化水素の溶解は、温度や圧力などの他の要因の影響を受けます。一般に、過酸化水素の溶解度は、温度の上昇とともに増加し、圧力が上昇すると低下します。より高い温度では、水分子の運動エネルギーの増加は、過酸化水素分子間の分子間相互作用を克服し、より高度な溶解につながります。一方、より高い圧力は、過酸化水素クラスターの形成を支持し、溶解度が低下します。