ヒ素はa -3イオン(as³⁻)を形成します 。その理由は次のとおりです。
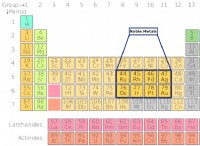
* グループ5: グループ5の要素には、5つの原子価電子(最も外側のシェルの電子)があります。
* 安定性: 原子は、安定した電子構成を実現するために電子を獲得または失う傾向があり、多くの場合、最も近い貴族に似ています。
* オクテットルール: オクテットのルールは、原子が8つの原子価電子を持っている場合に最も安定していると述べています。
* ヒ素の行動: 安定したオクテットを達成するために、ヒ素は3つの電子を獲得する可能性が最も高く、-3電荷(as³⁻)でイオンを形成します。