その理由は次のとおりです。
* 電気分解: このプロセスでは、電気を使用して、非種子化学反応を促進します。
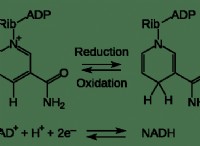
* カソード: 還元(電子のゲイン)が発生する負の電極。
* アノード: 酸化(電子の損失)が発生する正の電極。
ブライン電解では、次の反応が発生します。
* カソード(還元):
* 2H2O(L) + 2E-→H2(g) + 2OH-(aq)
* na +(aq) + e-→na(s)
* アノード(酸化):
* 2cl-(aq)→Cl2(g) + 2e-
カソードでは両方の反応が可能ですが、水の減少は標準の削減の可能性が低いため好まれています。ただし、水銀カソードの存在は、ナトリウムイオンの還元電位を大幅に低下させる可能性があるため、主要な種が減少します。
したがって、ナトリウムイオンはナトリウム金属に還元されます カソードでは、特に水銀カソードが使用されている場合、塩水の電気分解中。