1。極性: 水分子は極性です。つまり、わずかに正の末端(水素原子)とわずかに負の末端(酸素原子)があります。
2。アトラクション: 水分子(水素)の正の端は、負に帯電したcl-イオンに引き付けられます。同様に、水分子(酸素)の負の端は、正に帯電したNa+イオンに引き付けられます。
3。周辺: 複数の水分子が各イオンを囲み、水和シェルを形成します。イオンと水分子の間の静電引力は、結晶格子のイオン間の引力を克服するのに十分な強さです。
4。解離: 水分補給プロセスの結果、Na+およびCl-イオンは互いに分離され、水分子に囲まれています。彼らは今、解決策で独立して自由に移動することができます。
キーテイクアウト:
* 水分補給: イオンを取り巻く水分子のプロセスは、水和と呼ばれます。
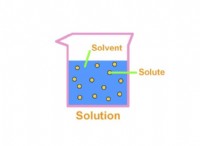
* 溶媒和: 溶質(塩など)を溶媒(水など)に溶解する一般的なプロセスは、溶媒和と呼ばれます。
* 静電引力: イオンと水分子の間の魅力は、静電力に基づいています。
* 解離: 溶液中で分離するイオンのプロセスは、解離と呼ばれます。
この水分補給と解離のプロセスは、塩が水に溶ける理由であり、それを良好な電解質にします。遊離イオンは電気を導入できます。