化学では、モル質量 1 モルあたりのグラム数 (g/mol) または 1 モルあたりのキログラム数 (kg/mol) で表した物質の質量です。モル質量は物質の集中的な特性です。つまり、その値はサンプル サイズに依存しません。
モル質量の求め方
化合物のモル質量を見つけるには、次の簡単な手順に従ってください:
- 化学式から始めます。
- 周期表を使用して、式中の各元素の原子質量を調べます。 (注:既知の同位体を使用している場合は、別の値を使用してください。)
- 化学式に従って、各元素の原子質量値を合計します。各元素について、原子質量にその記号の後に添え字を掛けます。下付き文字がない場合は、「1」を掛けることと同じです。
例 #1:元素のモル質量を求める
たとえば、ナトリウム 1 モルの質量を求めます。これを行うには、周期表でナトリウム (Na) を調べます。相対原子質量は、モル質量と同じです (ただし、モル質量は g/mol です)。ナトリウムのモル質量は 22.99 g/mol です。さて、ナトリウムの原子番号が 11 であることはわかっているので、なぜモル質量が正確に 22 でないのか (陽子 11 個と中性子 11 個) を不思議に思うかもしれません。これは、地球の地殻におけるナトリウムの平均同位体存在量には、ナトリウム 22 以外の同位体が含まれているためです。モル質量は平均であることを忘れないでください 1 モルあたりの質量。
別の例として、酸素ガス 1 モルの質量を求めます。酸素ガスは二原子分子 (O2 )。まず、元素の原子量 (原子量) を調べます。これは 16.00 です。次に、この値に 2 (酸素の記号 O に続く下付き文字) を掛けます。 O2 のモル質量 は 16.00 x 2 =32.00 g/mol です。
例 #2:NaCl のモル質量を求める
同じ手順を適用して、食卓塩または NaCl のモル質量を求めます。
<オール>例 #3:CO2 のモル質量を求める
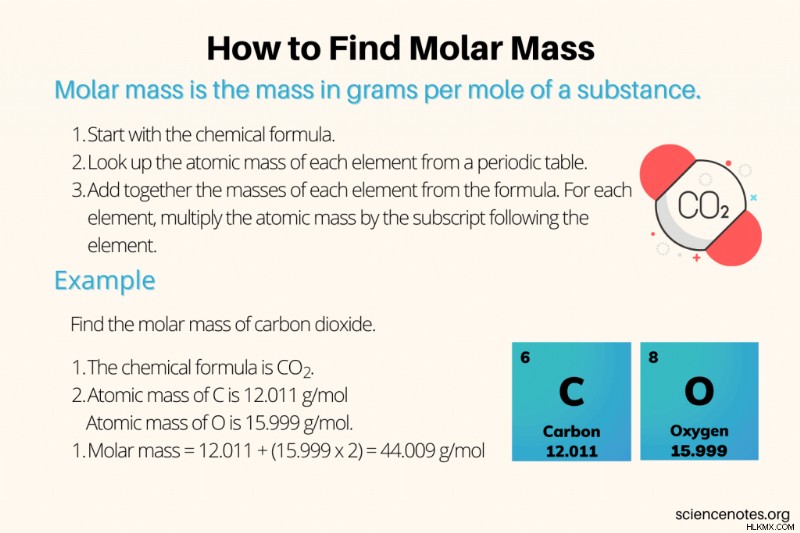
二酸化炭素のモル質量を求めます:
<オール>モル質量と分子質量
ほとんどの場合、人々は「モル質量」と「分子量」という用語を同じ意味で使用しています。しかし、両者はまったく同じではありません。
まず、分子量は単位がないか、ダルトン (Da) または原子質量単位 (amu または u) で報告されます。一方、モル質量の単位は、1 モルあたりのグラム数 (g/mol) または 1 モルあたりのキログラム数 (kg/mol) です。
第二に、分子量は、単一の分子または分子の種類の質量を表します。一方、モル質量はバルク特性であり、材料中の粒子の平均質量を反映しています。言い換えれば、元素の平均化学式と同位体比が重要です。
そのため、NaCl のモル質量は、元素の同位体存在量がわずかに異なるため、地球からのサンプルと金星で収集されたサンプルではおそらく異なります。より一般的なシナリオは、異なる数のモノマー サブユニットを含むポリマーのサンプルのモル質量を計算することです。モル質量のもう 1 つの用途は、さまざまな数の異なるヌクレオチドを含む DNA または RNA の 1 モルあたりの平均質量を求めることです。モル質量は、分子量が適用されない混合物に価値があります。
参考文献
- International Union of Pure and Applied Chemistry (1993)。 物理化学における量、単位、記号 (第 2 版)。オックスフォード:ブラックウェル科学。 ISBN 0-632-03583-8.
- IUPAC (1997)。 「相対モル質量」。化学用語集 (「ゴールド ブック」) (第 2 版)。オックスフォード:Blackwell Scientific Publications。 doi:10.1351/goldbook.R05270
- 国際度量衡局 (2006 年)。 国際単位系 (SI) (第8版)。 ISBN 92-822-2213-6.
- ポッソロ、アントニオ。 van der Veen, Adriaan M.H.;メイジャ、ジュリス。ヒバート、D. ブリン (2018)。 「標準原子量の不確かさの解釈と伝播 (IUPAC テクニカル レポート)」。 純粋化学と応用化学 . 90 (2):395–424. doi:10.1515/pac-2016-0402