1。既存の債券の破壊:
* 反応物: 化学反応の出発材料には、原子をまとめる化学結合の独自のセットがあります。
* エネルギー入力: これらの既存の結合を破るにはエネルギーが必要です。このエネルギーは、熱、光、電気などのさまざまなソースから生まれます。
2。再配置原子:
* 衝突と活性化エネルギー: 反応物は、結合強度を克服し、バラバラになるのに十分なエネルギー(活性化エネルギー)と衝突します。
* 中間種の形成: 原子と断片は、反応中に不安定な中間状態で一時的に存在する可能性があります。
3。新しい絆の形成:
* アトラクション: 壊れた結合からの原子と断片は再配置され、電気陰性度やその他の要因に基づいて新しいアトラクション(結合)を形成します。
* 製品形成: これにより、製品と呼ばれる新しい、より安定した分子が形成されます。
重要な概念:
* エネルギー保存: 化学反応は、エネルギーの保存法則に従います。システムの総エネルギー(反応物と生成物を含む)は一定のままです。
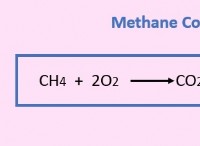
* 発熱と吸熱: 反応は、エネルギー(発熱、燃焼燃料など)を放出するか、エネルギー入力(光合成のような吸熱)を必要とする場合があります。
例:
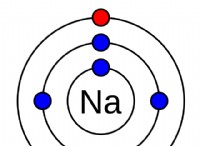
ナトリウム(Na)と塩素(Cl)の間の反応を考えて、塩化ナトリウム(NaCl)を形成します。
* 反応物: NAには単一の外部電子があり、Clには7があります。
* 債券破壊: 塩素原子を一緒に保持する結合は壊れます。
* 再配置: ナトリウム原子は、その外側の電子を失い、正に帯電したイオン(Na+)になります。塩素原子は電子を獲得して負に帯電したイオン(Cl-)になります。
* 新しい結合形成: イオンの反対の電荷が引き付けられ、イオン結合が形成され、安定した化合物NaCl(表塩)が生成されます。
要するに、化学反応には、反応物中の原子間の既存の結合の破壊と、異なる化合物(製品)を作成するための新しい結合の形成が含まれます。