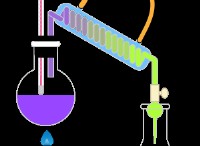
極性溶媒
* 定義: 極性溶媒は、電子の不均一な分布のために正と負の端を持つ分子を持っています。これにより、分子の片側に部分的な正電荷が生成され、もう片方に部分的な負電荷が生成されます。これらの料金のために「磁気」引力を持っていると考えてください。
* 例: 水(h₂o)、エタノール(c₂h₅oh)、アセトン(ch₃coch₃)
* なぜ重要なのか: それらは、極性分子とイオン化合物を効果的に溶解します。 「好きなようなような」と考えてください - 極性溶媒は他の極性物質で最適に機能します。
非極性溶媒
* 定義: 非極性溶媒には、電子の均一な分布を持つ分子があるため、明確な正または負の側面はありません。分子間力が弱いため、他の分子にあまり惹かれていません。
* 例: ヘキサン(c₆h₁₄)、ジエチルエーテル(c₄h₁₀o)、オイル
* なぜ重要なのか: 彼らは、脂肪や油などの非極性分子を溶解します。また、いくつかの有機化合物にとって良い溶媒である傾向があります。
これを視覚化する簡単な方法です:
* 磁石を想像してください: 極性溶媒は磁石のようなもので、他の磁石(極地分子)に引き付けられますが、非磁性材料(非極性分子)には強く引き付けられません。
* 金属片を想像してください: 非極性溶媒は金属片のようなもので、磁石(極分子)に引き付けられていませんが、他の金属(非極性分子)と相互作用することができます。
重要な注意:
*すべての分子が「極」または「非極性」カテゴリにきれいに適合するわけではありません。一部の分子には、極部と非極性部分の両方があります。
*極性の程度が重要です。一部の溶媒は他の溶媒よりも極性です。
より多くの例や説明が必要な場合はお知らせください!