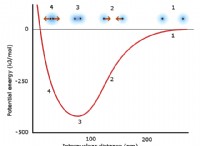
液体水(0°C以上):
* 高動態エネルギー: 液体の水分子は高速エネルギーが高く、迅速に動き回り、所定の位置に固定されていません。
* ランダムモーション: 分子はランダムな方向に移動し、頻繁に互いに衝突します。
* 水素結合: 水分子は水素結合を通じて互いに引き付けられますが、これは弱いが多数です。これらの結合は常に形成され、壊れており、分子が自由に動くことができます。
凍結(0°Cで):
* 運動エネルギーの損失: 水が冷えると、その分子は運動エネルギーを失います。 彼らは遅くなります。
* 結晶構造の形成: 温度が0°C(32°F)に達すると、分子は十分に遅くなり、水素結合がより安定して組織化されます。彼らは、クリスタルと呼ばれる通常の六角形の格子構造に自分自身を配置します。
氷(0°C未満):
* 低動態エネルギー: 氷の水分子は非常に低い運動エネルギーを持っています。それらは基本的にクリスタル構造内でその所定の位置に振動しています。
* 強い水素結合: 氷の水素結合は強く、結晶格子内の固定位置に分子を保持します。
* 分子運動の減少: 分子は、ランダムに自由に動き回ることができなくなりました。それらの動きは非常に制限されており、わずかに振動するだけです。
キーポイント:
* 密度の変化: 氷の結晶構造は水分子の間により多くの空間を残すため、氷は液体の水よりも密度が低くなります。これが氷が浮かぶ理由です!
* 相変化: 凍結は相変化であり、分子構造の変化により液体水が固体氷に移行します。
他に質問がある場合はお知らせください!