可溶性化合物:
* 塩: テーブル塩(NaCl)のようなほとんどの塩は、水に容易に溶解します。
* 砂糖: グルコースやフルクトースのような単純な糖は簡単に溶解します。
* 酸: 塩酸(HCl)や硫酸(H₂SO₄)などの多くの酸は、水に非常に溶けています。
* ベース: 水酸化ナトリウム(NaOH)や水酸化カリウム(KOH)などの多くの塩基も非常に溶けやすいです。
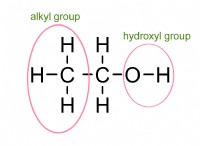
* エタノール: アルコールは、エタノールのように水と混和します。つまり、あらゆる割合で混ぜることができます。
溶解度に影響する要因:
* 極性: 水は極性分子です(一方の端はわずかに正、もう一方の端はわずかに陰性です)。 塩や砂糖など、水と同様の極性のある物質はよく溶けます。オイルのような非極性物質は、そうではありません。
* 温度: 一般に、温度を上げると、ほとんどの固形物の溶解度が向上します。
* 圧力: 圧力は、液体のガスの溶解度に大きな影響を与えます。より高い圧力は溶解度を高めます。
水に溶解する一般的な物質の例:
* 塩(NaCl)
* シュガー(c₁₂h₂₂o₁₁)
* 酢(酢酸)
* 重曹(重炭酸ナトリウム)
* 石鹸
* 洗剤
* コーヒー
* お茶
* ジュース
* 多くの薬
水に溶けないもの:
* 油と脂肪 (非極性)
* 砂
* プラスチック
* wood
覚えておいてください: 溶解は、多くの要因に影響される複雑なプロセスです。一部の物質は部分的にのみ溶解し、特定の温度でどれだけの溶質を溶解できるかに制限のある溶液を形成します。