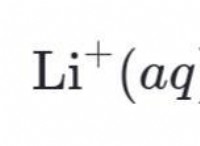反応:
hno₃(aq) + koh(aq)→kno₃(aq) +h₂o(l)
説明:
* 反応物:
*hno₃:硝酸、強酸。
* KOH:強酸カリウム、強い基部。
* 製品:
*Kno₃:硝酸カリウム、塩。
*H₂O:水、塩基からの水素イオン(H+)と水酸化物イオン(OH-)の組み合わせによって形成された水。
正味イオン方程式:
正味のイオン方程式は、反応に直接関与する種に焦点を当てています。
h⁺(aq) +oh⁻(aq)→h₂o(l)
キーポイント:
*反応は発熱性であり、熱を放出します。
*結果のソリューションは、強酸と強いベースが互いに中和するため、ニュートラル(7に近いpH)になります。
*この反応は、反応物の正と陰性のイオンがパートナーを切り替える二重変位反応の一般的な例です。