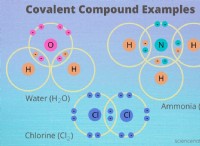
* 酸素の電子構成: 酸素には外側のシェルに6つの電子があり、さらに2つの電子がオクテットを完成させたいと考えています。
* 共有結合: 酸素は2つの水素原子を持つ2つの共有結合を形成し、安定性を達成するために電子を共有します。
* 孤立ペア: 酸素には2つの孤立した電子ペアがあり、結合ペアを撃退します。
* vsepr理論: 価数シェル電子ペア反発理論は、中心原子の周りの電子ペア(結合と孤立ペアの両方)が反発を最小限に抑えるために自分自身を整えると述べています。
これがどのように機能するかです:
1. O-H結合の電子の2つの結合ペアは、可能な限り離れて、104.5°の結合角を作成したいと考えています。
2。酸素の孤立ペアも負に帯電して結合ペアを撃退し、水素原子をさらに近づけます。
3。この反発は、完全な四面体構造ではなく、曲がった形になります。
このように考えてみてください:
水素原子を表す2つの弦が付いたバルーンを想像してください。風船自体は、その孤立ペアを持つ酸素原子を表します。弦は風船の圧力によって近づき、形を曲げます。
形状の重要性:
この曲がった形状は、水のユニークな特性にとって重要です。
* 極性: 曲がった構造は極性分子を作成し、酸素側にわずかに負の電荷と水素側にわずかに正電荷がかかります。
* 水素結合: 極性により、水分子は互いに水素結合を形成し、その高い沸点、表面張力、および溶媒特性につながります。
したがって、水分子は完全な四面体ではありませんが、その曲がった形状は電子反発の結果であり、水を必須の液体にする上で重要な役割を果たします。