ボラティリティの理解
* ボラティリティ 物質が液体からガスに簡単に変化することを指します(蒸発)。これは、物質の蒸発傾向の尺度です。
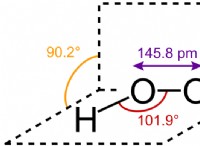
* 分子間力: (水中の水素結合など)分子を一緒に保持する力の強度は、ボラティリティに影響します。弱い力は、分子がより簡単に逃げることを意味します。
* 蒸気圧: 液体の上に蒸気がかける圧力は、揮発性の良い指標です。蒸気圧が高いということは、物質が容易に蒸発することを意味します。
なぜ一部の物質が水よりも速く蒸発する
1。分子間力が弱い: 分子間力が弱い物質は、より速く蒸発します。例えば:
* アセトン: アセトンは、水の強い水素結合と比較して、双極子双極子の相互作用が弱い。
* エタノール: エタノールには水素結合がありますが、水中の結合よりも弱いです。
* ガソリン: ガソリンは、非常に弱いファンデルワールスの力を持つ炭化水素の混合物です。
2。蒸気圧が高くなる: 蒸気圧が高い物質は、より速く蒸発します。これは、彼らが気相に逃げる傾向が高いことを意味します。
例
* アセトン: アセトンは容易に蒸発し、皮膚に冷却効果を残します。なぜなら、その弱い力により迅速に蒸発することができるからです。
* ガソリン: ガソリンは非常に迅速に蒸発するため、非常に可燃性です。
* エーテル: ジエチルエーテルは非常に速く蒸発するため、皮膚に塗布すると凍傷を引き起こす可能性があります。
蒸発速度に影響する要因
* 温度: 温度が高いほど、分子の運動エネルギーが増加し、蒸発が速くなります。
* 表面積: より大きな表面積は、より多くの液体分子を空気にさらし、蒸発を増加させます。
* エアフロー: 空気を動かすと、液体の上から蒸気分子が除去され、蒸発が増えます。
キーテイクアウト:
一部の物質が水よりも速く蒸発する理由は、分子間力とより高い蒸気圧が原因であるためです。 これらの要因により、分子が気相に逃げやすくなります。