* 運動エネルギーと衝突: 化学反応は、分子が既存の結合を破り、新しい結合を形成するのに十分なエネルギーと衝突すると起こります。 温度を下げると、分子の平均運動エネルギーが低下します。 これは、動きが遅くなり、衝突が少なく、力が少ないことを意味します。
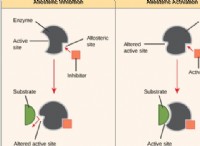
* 活性化エネルギー: すべての反応には活性化エネルギーがあり、反応が発生するのに必要な最小エネルギーです。 温度が低いと、この障壁を克服するのに十分なエネルギーがある分子が少ないことを意味します。
例外:
ほとんどの反応は低温で遅くなりますが、いくつかの例外があります。
* 発熱反応: 一部の反応は熱(発熱)を放出します。これらの場合、温度を下げると、活性化エネルギーを克服するために必要な熱が得られるため、実際には反応を *スピードアップ *します。
* 平衡反応: 可逆反応の場合、温度を下げると、均衡が熱を放出する側に向かって移動する可能性があります(発熱側)。これにより、速度定数が実際に減少しているにもかかわらず、反応が高速化されているように見えるようになります。
全体:
温度を下げると、一般に化学反応が遅くなります。これは、運動エネルギーの減少と、活性化エネルギーバリアを克服するのに十分なエネルギーを持つ分子の数の減少によるものです。ただし、特に発熱反応と平衡反応に関するいくつかの例外があります。