金属原子:
* ゆるくバインド: 原子価電子として知られる外側の電子は、核にゆるく結合されています。これは、金属構造全体で簡単に自由に取り外して移動できることを意味します。
* 電子の海: これらの自由移動電子は、正に帯電した金属イオンを囲む「電子の海」を作り出します。この「海」は、導電率や閉鎖性など、金属のユニークな特性の多くを担当しています。
* 非局在: 価電子は特定の原子に関連していませんが、金属格子全体で共有されます。
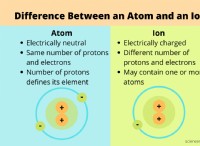
* 簡単に失われました: 金属原子は原子価電子を失い、陽イオン(陽イオン)を形成する傾向があります。
非金属原子:
* しっかりと結合: 非金属原子には、原子核にしっかりと結合している原子価電子があります。それらは簡単に分離または共有されません。
* ローカライズ: これらの電子は、それぞれの原子に特異的に関連しており、他の原子と共有されていません。
* 電子ゲイン: 非金属は、安定した電子構成を実現するために電子を獲得する傾向があり、負イオン(アニオン)を形成します。
これらの違いが金属と非金属の特性にどのように影響するかは次のとおりです。
* 導電率: 金属の自由移動電子は、電気と熱を簡単に伝達できるようにします。しっかりと結合した電子を備えた非金属は、導体が不十分です。
* 柔軟性と延性: 金属中の電子の海は、金属イオンが構造を壊すことなく互いに通り過ぎることを可能にし、閉鎖性(シートにハンマーされる能力)と延性(ワイヤに引き寄せる能力)につながります。非金属は一般に脆く、簡単に壊れます。
* 光沢: 金属の遊離電子は光を反射し、光沢のある外観(金属光沢)を与えます。非金属にはこの特徴がありません。
* 化学結合: 金属は、電子を非金属に失うことにより、イオン結合を形成する傾向があります。非金属は、他の非金属と電子を共有することにより、共有結合を形成します。
要約: 重要な違いは、価電子の可動性と結合強度にあります。 金属原子にはゆるく結合された非局在電子があり、非金属原子にはしっかりと結合された局所的な電子があります。この根本的な違いは、物理的および化学的特性が大きく異なることにつながります。