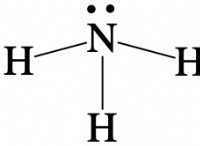
* ルイス構造は、価電子に焦点を当てています。 価電子は、原子の最も外側の殻の電子であり、結合に関与しています。
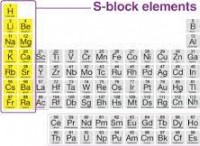
* ナトリウムには1つの価電子のみがあります。 ナトリウムの電子構成は1S²2s²2pp⁶3S¹です。つまり、最も外側のシェル(3S軌道)に1つの電子があります。
* ルイス構造は、ドットを使用して価電子電子を表します。 ナトリウム原子には1つのドットしかありません。
したがって、ナトリウムのルイス構造は、その孤立価の電子を表す単一のドットです。結合や孤独なペアが表示されないため、典型的なルイス構造ではありません。
ルイス構造の代わりに、このようなナトリウムの電子構成の単純化された表現が表示される場合があります。
NA:•
これは、ナトリウムが1つの価電子を持っていることを示しています。