* 銅(ii)イオンの電子構成: 銅(II)にはd⁹電子構成があります。つまり、そのd軌道に1つの対応のない電子があります。
* リガンドフィールド分割: リガンド(水や塩化物イオンなど)がCu²⁺イオンに近づくと、D軌道と相互作用し、異なるエネルギーレベルに分かれます。この分割は、リガンドフィールド分割として知られています 。
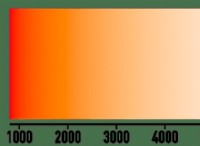
* D-D遷移: 対応のない電子は、エネルギーを吸収し、より高いエネルギーD軌道にジャンプできます。この吸収は、電磁スペクトルの可視領域、特にオレンジの赤波長で発生します。
* 補完的な色: 銅(II)イオンはオレンジ色の光を吸収するため、相補的な色 、これは青です 、送信されて反射され、溶液に特徴的な青色の色を与えます。
色に影響する要因:
* リガンドタイプ: 異なるリガンドは、異なる程度のリガンドフィールド分割を引き起こし、銅塩の色に影響を与える可能性があります。たとえば、銅(II)硫酸銅(Cuso₄)は溶液中の淡い青色ですが、塩化銅(Cucl₂)は緑がかった青です。
* 濃度: 青色の強度は、銅(II)イオンの濃度に依存します。
* 溶媒: 溶媒は、Cu²⁺イオンとリガンドの間の相互作用を変えることにより、色に影響を与える可能性があります。
例外:
ほとんどの銅(II)塩は青ですが、次のようないくつかの例外があります。
* 銅(i)塩: 銅(i)塩(cu⁺)は通常、D-dの遷移を防ぐD軌道が満たされているため、無色または白です。
* 強く色のリガンドを備えた銅塩: シアン化物や硫化物のような一部のリガンドは、銅の塩の色を支配できる独自の強い色を持つことができます。
要約すると、銅塩の青色は銅(II)イオンと周囲のリガンドとの相互作用の結果であり、D-D遷移と可視光の特定の波長の吸収につながります。