本当のこと:
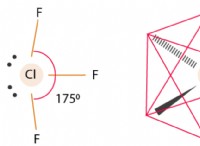
* 電気陰性度: 塩素(Cl)は、水素(H)よりも電気陰性です。これは、塩素が結合中の共有電子をより強く引っ張っていることを意味します。
* 極性共有結合: 塩素と水素の間の電気陰性度の違いは、極性共有結合を生成します 。塩素原子はわずかに負電荷(Δ-)を持ち、水素原子にはわずかに正電荷(Δ+)があります。
間違っているもの:
* 非極性共有分子: 声明は、塩化水素(HCl)が非極性であると誤って結論付けています。 極性結合結合により、HClは極分子です。
なぜHClが極性であるのか:
電子の不均一な共有は、HCl分子に永久双極子モーメントを作成します。塩素の端はより陰性であり、水素端はより陽性です。この電荷の分離は、分子極になります。
要約:
* HClは、水素と塩素の間の極性共有結合のために極性分子です。 共有電子の塩素原子の強い引っ張りは、塩素端に部分的な負電荷を作成します。