これが故障です:
水(h₂o):
*酸素には、2つの孤立した電子と水素原子の2つの結合ペアがあります。
*唯一のペアは、電子密度が高く、局所性の低い性質により、結合ペアよりも強い反発力を発揮します。
*この反発により、結合ペアが互いに近づき、 104.5°の結合角度が小さくなります。 。
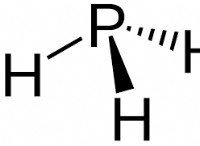
アンモニア(nh₃):
*窒素には、1つの孤立ペアと水素原子と3つの結合ペアがあります。
*孤独なペアは再び結合ペアを押し込み、結合角を 107°に減らします 。
要約:
水とアンモニアの中心原子に孤立したペアが存在すると、理想的な四面体角と比較して結合角が減少します。これは、唯一のペアが結合ペアよりも大きな反発力を持ち、結合ペアを近づけることを強制するためです。