1。価電子電子をカウント
* 酸素(O): 6価電子/原子 * 2原子=12電子
* 炭素(c): 4価電子/原子 * 2原子=8電子
* 水素(H): 1価電子/原子 * 6原子=6電子
総価電子電子: 12 + 8 + 6 = 26電子
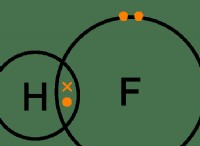
2。ルイス構造を描きます
* スケルトン: 単一の結合で接続された炭素原子から始めます:C-C
* 水素を取り付ける: 各炭素は、H-C-C-Hの2つの水素原子を取得します
* 酸素を取り付ける: 各炭素は、1つの酸素原子、H-C-O-C-Hを取得します
* 孤立ペアを追加: 各酸素原子は、オクテットを完成させるために2つの孤立ペアを必要とします。
ルイス構造:
`` `
h h
| |
C c
/ \ / \
h o h h
| |
h h
`` `
3。結合ペアと非結合ペア
* 結合ペア: 各結合(シングルまたはダブル)は、電子の1つの結合ペアを表します。構造には合計7つの結合があります。
* 非結合ペア: 酸素原子の各孤立ペアは、1つの非結合ペアを表します。合計4つの孤独なペアがあります。
概要:
* 総価電子電子: 26
* 結合ペア: 7
* 非結合ペア: 4