水素結合:
* 水: 水分子は非常に極性であり、つまり、正の端(水素原子)と負の端(酸素原子)があります。これらの反対の電荷により、水分子は互いに強い水素結合を形成することができます。これらの結合は非常に強く、壊れるのに多くのエネルギーが必要であり、なぜ水が室温で液体のままであるのかを説明しています。
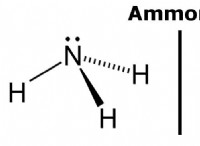
* アンモニア: アンモニアには極構造もあり、水素結合を形成しますが、水中の構造よりも弱いです。これは、アンモニアの窒素原子が水中の酸素原子よりも電気陰性ではないため、共有電子にはそれほど強く引っ張らないためです。より弱い水素結合は、それらを破壊するために必要なエネルギーが少ないことを意味するため、アンモニアは室温でガスとして存在します。
その他の要因:
* 分子量: 水素結合ほど重要ではありませんが、アンモニアは水よりも分子量が少ないため、その揮発性にも寄与します(気化する傾向)。
要約: 重要な違いは、水素結合の強度にあります。水の強い水素結合は、室温での沸点と液体状態が高くなりますが、アンモニアの弱い水素結合は、沸点が低く、室温で気体状態になります。