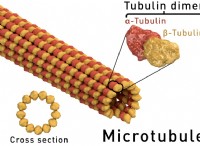
その理由は次のとおりです。
* 両性酸化物 酸と塩基の両方として作用できる金属酸化物です。
* 酸 溶液中に水素イオン(H+)を寄付します。
* アルカリ 溶液中に水酸化物イオン(OH-)を寄付する塩基です。
酸との反応
両性酸化物が酸と反応すると、塩基として機能し、塩と水を形成するために水素イオンを受け入れます。
例:
酸化アルミニウム(Al2O3)は塩酸(HCl)と反応します。
AL2O3(s) + 6hcl(aq)→2alcl3(aq) + 3h2o(l)
ここでは、塩化アルミニウム(ALCL3)が形成された塩です。
アルカリとの反応:
両性酸化物がアルカリと反応すると、酸として機能し、酸化物イオン(O2-)を寄付して塩と水を形成します。
例:
酸化アルミニウム(Al2O3)は、水酸化ナトリウム(NaOH)と反応します。
AL2O3(s) + 2NAOH(AQ) + 3H2O(L)→2NAAL(OH)4(AQ)
ここでは、アルミン酸ナトリウム(Naal(OH)4)が形成された塩です。
両性酸化物の一般的な例:
*酸化アルミニウム(AL2O3)
*酸化亜鉛(ZNO)
*酸化鉛(PBO)
したがって、酸化アルミニウムのような酸化酸化酸化酸化酸化物は、酸とアルカリの両方と反応して、塩水(および別の塩)を形成します。