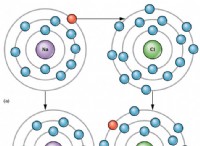
* イオン化合物: 塩化カルシウムはイオン化合物であり、積極的に帯電したカルシウムイオン(Ca²⁺)と負に帯電した塩化物イオン(Cl⁻)との間の静電引力によって形成されます。
* 固体状態: 固体状態では、これらのイオンは結晶格子に硬く保持され、自由に動くことを防ぎます。これが、固体塩化カルシウムが貧弱な導体である理由です。
* 溶融状態: 塩化カルシウムが溶けると、イオンを保持する強力な静電力が克服されます。イオンは液体内でランダムに動き回ることができます。
* 電気伝導率: 塩化溶融カルシウム全体に電位が加えられると、遊離カルシウムイオンは負の電極(カソード)に向かって移動し、遊離塩化物イオンは正の電極(アノード)に向かって移動します。荷電粒子のこの動きは、電流を構成します。
要約すると、塩化溶融カルシウムの導電率は、その構成イオンのモバイル、電荷を運ぶ液体への解離によるものです。