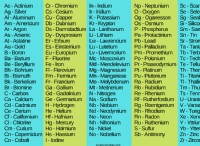
* カルシウムイオン(ca²⁺) :カルシウム原子が2つの電子を失うと形成される正の帯電イオン。
* 塩化物イオン(Cl⁻) :塩素原子が1つの電子を獲得すると、負に帯電したイオンが形成されます。
CaCl₂では、カルシウムイオン(Ca²⁺)ごとに2つの塩化物イオン(Cl⁻)があります。この配置により、化合物の全体的な電荷が中性であることが保証されます。
化合物イオン 正味の正または負の電荷とともに結合した複数の原子で構成される多原子イオンです。例は次のとおりです。
* 硫酸イオン(so₄²⁻)
* 硝酸イオン(no₃⁻)
* アンモニウムイオン(nh₄⁺)
したがって、CaCl₂は化合物イオンではなく、単純なイオンの組み合わせによって形成されるイオン化合物です。