触媒は物質であり、化学反応に追加されると、進行中の化学反応の速度を変更または変更します。言い換えれば、触媒はあらゆる化学反応の律速因子です。触媒には、正と負の 2 種類があります。
正の触媒は反応速度を上げて反応速度を変化させ、負の触媒は反応速度を低下させて化学反応を変化させます。
積極的な触媒
触媒の定義から、触媒が実際の進行中の化学反応速度を変化させることがわかっています。 「正の触媒」という用語は、進行中の反応の速度を高めることにより、化学反応の速度にプラスの影響を与えることを示唆しています。可逆反応では、正の触媒は平衡位置を変えませんが、より短い時間で反応の平衡状態に到達しようとします。
正の触媒の働き
反応物分子は、化学反応を完了するための閾値エネルギー点に到達するための最小量のエネルギーを必要とします。閾値エネルギー点は、活性化された複合種が形成されるときです。ここで、反応物の部分結合と生成物の部分結合が存在するか、反応物と生成物の混合結合が存在する。この活性化された複合種は、最終的に反応の生成物に変換されます。
必要なエネルギー量は、活性化エネルギーとして知られており、エネルギー閾値に到達します。あらゆる化学反応に触媒が存在するとします。その場合、進行中の化学反応の元の活性化エネルギーよりも少ない活性化エネルギーと異なる種類の遷移状態を提供することにより、反応物分子への代替経路を提供します。最後に、その化学反応の速度を上げます。
触媒化学反応のプロセスでは、触媒は純粋に反応に関与するのではなく、反応するために反応物に表面積を提供するか、それ自体が反応する代替経路を提供するだけです。反応物は中間種を形成し、反応の完了後、反応の最初の期間に入れたのと同じ生成物と純粋な触媒が得られます。 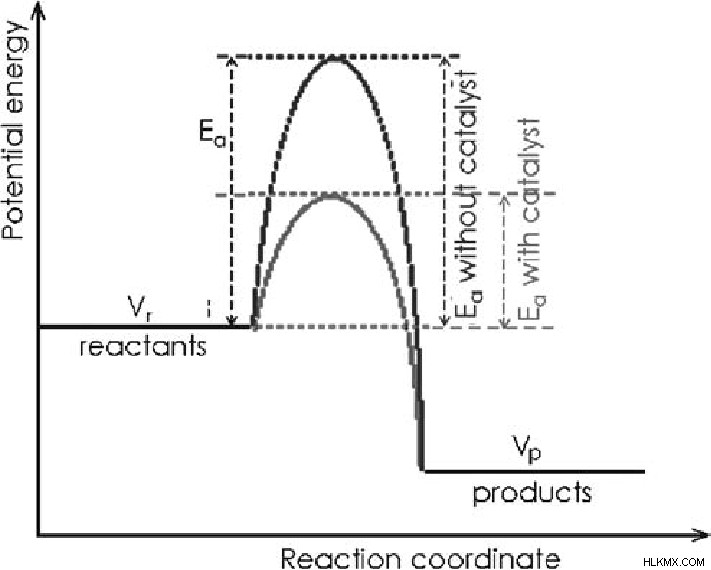
触媒の例
酵素は正の触媒のカテゴリに分類され、次のように人体内の化学反応の速度を高めるため、生物学的触媒として知られています:
H2CO3 (aq) ↔ H2O(l) + CO2(g)
- 上記の化学反応において、炭酸脱水酵素(H2CO3)は生体触媒であり、二酸化炭素(CO2)を吐き出すことで血液から肺への二酸化炭素(CO2)の拡散速度を高めます。非常に迅速に平衡状態に到達することにより、二酸化ガスが発生します。
過マンガン酸カリウム (KMnO4) は、過酸化水素 (H2O2) の化学反応の分解速度を速め、酸素ガス (O2) に変換する触媒でもあります。反応温度を上げて水 (H2O) を生成します。温度が上昇し、反応物分子の衝突速度と反応速度が上昇します。
多くの遷移金属は触媒としても機能し、プラチナ (Pt) のような多くの化学反応の速度を高めます。プラチナはコンバーターとして自動車に使用されています。
プラチナ ブラックは、酸素ガス (O2) と水素ガス (H2) が結合して水分子を形成する可能性を高めるため、正の触媒としても使用されます。
2H2 + O2 —(Pt)– 2H2O
窒素酸化物 (NO) は、SO2 から SO3 への酸化の化学反応速度を高めるもう 1 つの正の触媒です。
二酸化マンガンは、塩素酸カリウム (KClO3) の塩化カリウム (KCl) と酸素ガスへの分解速度を高めるため、正の触媒でもあります。ガス (O2) が解放されます。
2KClO3 (s) –−−(Δ, MnO2)−−→ 2KCl(s) + 3O2(g)
鉄 (Fe) は、アンモニア合成プロセスにおける積極的な触媒です。
ゼオライトは、石油分解プロセスにおける積極的な触媒です。
ニッケル、パラジウム、およびプラチナは、不飽和炭化水素の水素化プロセスにおける積極的な触媒です。
結論
正の触媒は、反応種によって消費されることなく、反応にのみ関与することによって進行中の化学反応の速度を高める物質です。関与する反応物の活性化エネルギーが低下するため、触媒の存在下での化学反応の速度は増加します。