安定性が重要な理由:
* 電子構成: 原子は、電子の完全な外側の殻を持っている場合、最も安定しています。この配置は、正に帯電した核と負に帯電した電子との間に可能な限り強力な引力を提供します。
* オクテットルール: ほとんどの原子では、この完全な外側シェルは8つの電子を持つことを意味します(オクテットルール)。 例外は、特に周期表(水素やヘリウムなど)の1列目と2列目の要素の場合があります。
原子が安定性を達成する方法:
* イオン結合:
* 電子の伝達: 1つ以上の電子がある原子から別の原子に伝達されます。
* イオンの形成: 電子を失う原子は正の帯電イオン(陽イオン)になり、電子を摂取する原子は負に帯電したイオン(アニオン)になります。
* 静電引力: イオンの反対の電荷が互いに引き付けられ、イオン結合が形成されます。
* 例: ナトリウム(Na)は電子を失い、Na+を形成しますが、塩素(Cl)は電子を獲得してCl-を形成します。これらのイオンは互いに引き付けて、塩化ナトリウム(NaCl)またはテーブル塩を形成します。
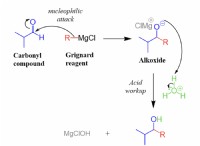
* 共有結合:
* 電子の共有: 2つ以上の原子が電子を共有して、完全な外側シェルを実現します。
* 共有結合: これらの共有電子は両方の原子の核に引き付けられ、共有結合が生じます。
* 共有結合の種類:
* 非極性共有結合: 電子は原子間で等しく共有されます。
* 極性共有結合: 電子は原子間で不均等に共有され、一方の原子に部分的な正電荷と他の原子に部分的な負電荷が生じます。
* 例: 2つの水素原子(H)は電子を共有して、水素分子(H₂)に非極性共有結合を形成します。
要約:
原子は、電子の完全な外殻を達成することにより、安定性を努力します。これは、電子の伝達(イオン結合)または電子の共有(共有結合)を通じて達成できます。 これらの結合は、すべての分子と化合物の形成の基本であり、物質の物理的および化学的特性を形成します。