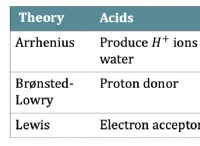
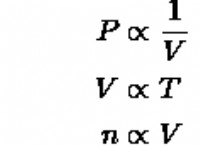1。電子構成:
* 価電子: 原子内の最も外側の電子は、価電子と呼ばれます。これらの電子は化学結合に関与しています。原子は、安定した電子構成、通常は完全な外側シェル(オクテットルール)を達成するために反応する傾向があります。
* 電気陰性度: これは、結合中に電子を引き付ける原子の能力の尺度です。電気陰性度の高い原子は電子を獲得する傾向がありますが、電気陰性度が低い原子は電子を失う傾向があります。
2。核電荷:
* 陽子の数: 核内の陽子の数は、原子数と正電荷の強度を決定します。より高い核電荷は電子をより強く引き付けます。
3。エネルギーレベルと軌道:
* エネルギーレベル: 電子は、原子内の特定のエネルギーレベルを占めます。原子は反応して、より低いエネルギー状態を達成します。
* 軌道: 電子は、エネルギーレベル内で特定の軌道を占有します。軌道の形状と方向は結合に影響します。
4。イオン化エネルギーと電子親和性:
* イオン化エネルギー: 原子から電子を除去するために必要なエネルギー。イオン化エネルギーが低い原子は、電子を失う傾向があります。
* 電子親和性: エネルギーは、電子が中性原子に加えられると変化します。電子親和性が高い原子は、電子を獲得する傾向があります。
5。化学結合の種類:
* イオン結合: 原子間の電子の伝達によって形成され、反対の電荷を持つイオンが生成されます。 これらの結合は通常、有意に異なる電気陰性度の原子間で発生します。
* 共有結合: 原子間の電子の共有によって形成されます。これらの結合は通常、同様の電気陰性度の原子間で発生します。
* 金属結合: 金属原子の間で発生します。そこでは、電子が金属格子全体で非局在化します。
6。その他の要因:
* 温度: 温度の上昇は、多くの場合、化学反応の速度を増加させます。
* 圧力: ガスを含む反応の場合、圧力の増加は、より少ないガス分子を生成する反応を支持する可能性があります。
* 触媒の存在: 触媒は、その過程で消費されることなく化学反応を高速化します。
要約すると、反応する原子の傾向は、その電子構成、核電荷、エネルギーレベル、および他の原子との安定した結合を形成する可能性に依存します。これらの要因は、原子がより安定した状態に到達するために電子を獲得、失い、または共有することができる方法を決定します。