1。コンポーネントを理解する:
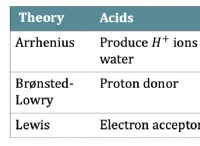
* 硫黄: 硫酸の中心原子。
* 水素(H): 名前の酸部分は、水素の存在を意味します。
* 酸素(O): 「硫酸」の「IC」接尾辞は、より高い酸化状態に酸素が存在することを示しています。
2。要素の組み合わせ:
* 水素: 酸には通常、溶液中のプロトン(H+)として放出できる1つ以上の水素原子があります。
* 硫黄: 硫黄は、硫酸中の+6の一般的な酸化状態を持っています。
* 酸素: 酸素は一般に-2の酸化状態を持っています。
3。酸化のバランス状態:
*中性化合物を達成するには、酸化状態の合計がゼロに等しくなければなりません。
*硫黄の+6酸化状態のバランスをとるには、2つの水素原子(各+1)が必要です。
*酸素の-2酸化状態のバランスをとるには、4つの酸素原子が必要です。
4。式:
それをすべてまとめると、硫酸の化学式はh₂so₄です 。