その理由は次のとおりです。
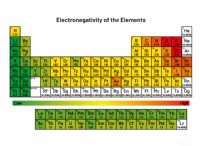
* 構造: Hclo4は過塩素酸です。それは、過塩素酸イオン(ClO4-)の高電気陰性酸素原子(O)に結合した水素原子(H)を持っています。
* 陽子寄付: Hclo4が水に溶解すると、水分子イオン(H+)を水分子に容易に寄付し、ハイドロニウムイオン(H3O+)を形成します。これが酸の特徴的な挙動です。
* ph: Hclo4の溶液は非常に低いpHを持ち、高濃度の水素イオン、したがって強酸性の性質を示しています。
要約すると、hclo4は溶液中に陽子(H+)を容易に寄付する能力のために強酸です。