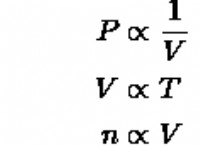溶解度
* 定義: 特定の温度と圧力で、特定の量の別の物質(溶媒)で溶解できる最大量の物質(溶質)。
* キーポイント:
*これは、定義された条件下で特定の溶質溶媒ペアの特性です。
*溶媒(または他のユニット)100グラムあたりの溶質グラムとして表されます。
*温度や圧力などの要因の影響を受ける可能性があります。
飽和
* 定義: 特定の温度と圧力で溶解した溶質の最大量を含む溶液。
* キーポイント:
*それは解決策の状態であり、物質の特性ではありません。
*飽和溶液に溶質を追加すると、溶解しません。それは沈殿するかもしれません。
*溶解度が低い飽和溶液または溶解度が高い飽和溶液を使用できます。
関係
* 溶解度が飽和度を決定します: 物質の溶解度は、飽和状態に到達するためにどれだけの溶質を溶解できるかを決定します。
* 飽和は、溶解度に関連する状態です: これらの条件でその溶質の溶解度の制限に達したとき、溶液は飽和します。
例
* 溶解度: 室温での水中の砂糖の溶解度は、100グラムあたり約200グラムです。
* 飽和: 100グラムの水に溶解した200グラムの砂糖を備えた溶液は、室温での飽和糖溶液です。より多くの砂糖を追加しても溶解しません。
要約:
* 溶解度: *溶解できる最大量。
* 飽和: 最大量 *が溶解するソリューションの状態。