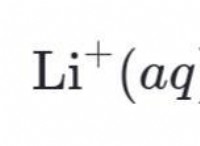反応
C2H5OH(エタノール) + H2SO4(硫酸)→C2H4(エチレン) + H2O(水)
メカニズム
1。エタノールのプロトン化: 硫酸は強酸として機能し、エタノールのヒドロキシル基(-OH)をプロトン化します。これにより、優れた退去グループ、水(H2O)が作成されます。
2。カルボンの形成: プロトン化されたエタノール分子は水を失い、カルボン(正電荷の炭素原子)を形成します。この場合、カルボンはエチルカルボン(CH3CH2+)です。
3。陽子の除去: プロトン(H+)は、カルボンに隣接する炭素原子から除去され、二重結合の形成とエチレンの放出につながります。
条件
* 温度: 反応には、通常は170°C前後の高温が必要です。これにより、脱水プロセスが促進されます。
* 硫酸の濃度: 硫酸の濃縮溶液を使用して、反応が効果的に進行するようにします。
* 追加率: 反応は発熱性であり、かなりの熱を発生させる可能性があるため、エタノールは硫酸にゆっくりと添加されます。
重要なメモ:
* 副反応: より高い温度では、他の副反応が発生する可能性があり、ジエチルエーテル(C2H5OC2H5)の形成につながります。
* 産業プロセス: この反応は、石油化学産業の重要なビルディングブロックである大量のエチレンを生産するために工業的に使用されます。
全体として、反応にはエタノールからの水分分子の除去が含まれ、エチレンと水が形成されます。このプロセスは、硫酸の強酸性特性と高温条件によって駆動されます。