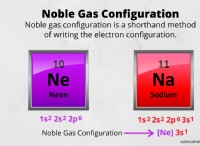
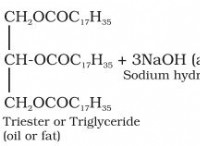* 共有結合: 窒素(N)および水素(H)原子は電子を共有してアンモニアの結合を形成します。この電子の共有は、共有結合の特徴です。
* 電気陰性度: 窒素は水素よりも電気陰性です。つまり、共有電子に強い引っ張りがあります。これにより、窒素原子に部分的な負電荷(Δ-)が生成され、水素原子に部分的な正電荷(Δ+)が生成されます。
* 分子形状: アンモニアは、頂点に窒素原子を含む三角錐体形状を持っています。窒素原子の孤立した電子のペアは、水素原子を押しのけ、偏った電荷分布をもたらします。
要約: 電気陰性度の違いと非対称分子形状による電子の不均等な共有により、アンモニアは極性分子になります。