* 鉄の反応性: 鉄は比較的反応性のある金属です。電解質(塩など)の存在下で酸素と水と容易に反応して、一般的に錆として知られている酸化鉄を形成します。
* 腐食の電気化学的性質: 腐食は、金属が電子を失い、イオンを形成する電気化学プロセスです。 鉄は、リストの他の金属よりもこのプロセスに起因する傾向があります。
* その他の要因: 腐食速度は、温度、湿度、不純物の存在などの要因の影響を受ける可能性があります。ただし、鉄の固有の反応性により、腐食を非常に受けやすくします。
他の金属を見てみましょう:
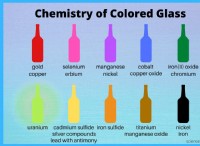
* 銅(Cu): 銅は、さらなる腐食を遅くする保護酸化物層(緑青)を形成します。
* リード(PB): 鉛はまた、さらなる腐食に抵抗する保護酸化物層を形成します。
* シルバー(Ag): 銀は変色します(黒い硫化物層を形成します)が、一般に腐食に耐性があります。
* アルミニウム(AL): アルミニウムは、腐食に対して非常に耐性のある薄い保護酸化物層を形成します。
* マグネシウム(mg): マグネシウムは容易に腐食しますが、他の金属を腐食から保護するための犠牲アノードとしてしばしば使用されます。
* 亜鉛(Zn): 亜鉛も腐食を起こしやすいが、他の金属の保護コーティングとしてよく使用される(亜鉛めっき)。
要約: リストにある他の金属は特定の条件下で腐食する可能性がありますが、鉄は、その反応性が高く、錆を形成する傾向があるため、腐食が発生しやすくなります。