普遍的な指標 は、幅広い pH 値にわたっていくつかの色の変化を表示する pH 指示薬です。リトマス試験紙や個々の pH 指示薬と同様に、普遍的な指示薬は溶液のアルカリ度の酸性度を示します。ただし、個々の染料は通常、狭い pH 範囲で色が変わりますが、一般的な指示薬は酸、中性溶液、および塩基に対して機能し、虹色全体に変化します.
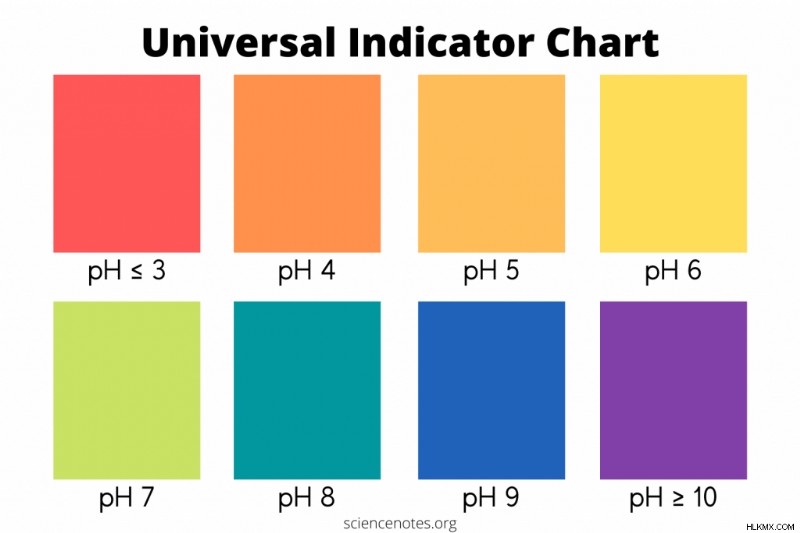
ユニバーサル インジケーター チャート
教室、研究室、または自宅で使用するために、ユニバーサル インジケーター チャートをダウンロードして印刷してください。この表は、一般的な指示薬溶液の典型的な色と pH 値を示しています:
| pH 範囲 | 説明 | 色 |
|---|---|---|
| <3 | 強酸性 | レッド |
| 3-4 | 酸性 | オレンジ |
| 5 | 弱酸 | 黄橙色 |
| 6 | 弱酸性 | イエロー |
| 7 | ニュートラル | 緑 |
| 8 | 弱アルカリ性 | 青緑 |
| 9 | 弱アルカリ | ブルー |
| >10 | 強アルカリ性 | バイオレット |
これらの色は、通常、チモール ブルー、メチル オレンジ、メチル レッド、ブロモチモール ブルー、およびフェノールフタレインであるユニバーサル インジケーターの色素間の相互作用から生じます。
| 指標 | 低pH色 | 遷移範囲 | 高pH色 |
|---|---|---|---|
| チモール ブルー (最初の遷移) | レッド | 1.2 – 2.8 | イエロー |
| メチルオレンジ | レッド | 3.2 – 4.4 | イエロー |
| メチルレッド | レッド | 4.8 – 6.0 | イエロー |
| ブロモチモール ブルー | イエロー | 6.0 – 7.6 | ブルー |
| チモール ブルー (2 番目の遷移) | イエロー | 8.0 – 9.6 | ブルー |
| フェノールフタレイン | 無色 | 8.3 – 10.0 | ピンクまたはレッド |
カラー チャートは実験の出発点として適していますが、インジケーター ソリューションを調整することをお勧めします。既知の pH 値の化学物質をテストして実際の色を記録します。

ユニバーサル インジケーターの作り方
ユニバーサル インジケーター ソリューションは、オンラインで簡単に入手できます。ただし、自分で作るのは簡単です。いくつかのユニバーサルインジケーターレシピがあります。ほとんどは 1933 年の山田の特許のバリエーションです。
クラシック ユニバーサル インジケーター ソリューションのレシピ
- メチルレッド
- フェノールフタレイン
- ブロモチモール ブルー
- 95% エタノール
- 蒸留水
指示薬溶液は密閉容器に保管してください。賞味期限は約 3 年です。
簡単なユニバーサル インジケーターのレシピ
このレシピではより多くのインジケーター染料を使用しますが、必要な手順は少なくなります.
- フェノールフタレイン 0.1 g
- 0.2 g メチルレッド
- メチル オレンジ 0.3 g
- ブロモチモール ブルー 0.4 g
- チモールブルー 0.5 g
ユニバーサル インジケーター ソリューションの保存期間は、密閉容器で約 3 年間です。
キャベツ ジュース ユニバーサル インジケーター レシピ
赤または紫のキャベツ ジュースを使用すると、経済的で毒性のない解決策になります。他のほとんどの天然 pH 指示薬とは異なり、キャベツ ジュースは幅広い色を示します。
<オール>キャベツジュースのインジケーターは、冷蔵庫で数週間、または使用するまで冷凍されている場合は無期限に持続します.この指標にはカラーチャートがありますが、各キャベツにはさまざまなアントシアニンの量がわずかに異なるため、独自に作成することをお勧めします.
ユニバーサルインジケーターpHペーパーを作る
万能指示薬があれば、pH紙の作成は簡単です。ろ紙を指示薬溶液に浸します。スポイトを使用してインジケータ溶液を適用すると、クリーンアップが簡単になります。紙を乾かしてから、テスト ストリップにカットします。
テストストリップを液体に浸さないでください!スポイトを使用して、ストリップの一方の端にテスト液を 1 滴垂らします。次に、色をグラフと比較します。
参考文献
- L. S. フォスター。 Gruntfest、I. J. (1937)。 「万能指標を使った実証実験」。 Journal of Chemical Education . 14 (6):274. doi:10.1021/ed014p274
- ラスーリ、ザーラ;アブドラヒ、ハミド。 Maeder、マルセル(2020)。 「溶液pHの一般化された指標ベースの決定」。 Analytica Chimica Acta . 1109:90-97. doi:10.1016/j.aca.2020.03.004
- シュヴァルツェンバッハ、ジェロルド (1957)。 複合滴定 .ハリー・アーヴィング訳(第1英語版)。ロンドン:Methuen &Co.
- ウォーカー、デニス (2007)。 酸とアルカリ (第 1 版)。ロンドン:エヴァンス。 ISBN 0-237-53002-3.
- Zumdahl, Steven S. (2009). 化学原理 (第6版)。ニューヨーク:ホートン ミフリン カンパニー。