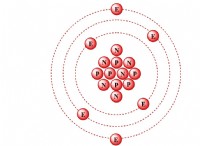
* 電子構成: アルカリ金属は、周期表のグループ1に属します。彼らは最も外側のシェルに単一の原子価を持っています。たとえば、ナトリウム(Na)には電子構成[ne]3s¹があります。
* 電子を失う傾向: 単一の原子価電子のため、アルカリ金属は、安定した貴重なガス構成を実現するためにこの電子を失う傾向が強いです。 1つの電子を失うと、非常に安定した状態である完全な外側のシェルが残ります。
* 酸化番号: 原子が電子を失うと、それは正に帯電します。失われた電子の数は、酸化数で表されます。アルカリ金属は1つの電子を失うため、酸化数は+1です。
例:
*ナトリウム(Na)は1つの電子を失い、酸化数が+1のNaです。
概要:
その電子構成(1つの原子価電子)と安定性を達成するためにその電子を失う傾向の組み合わせは、酸化数が+1のアルカリ金属の結果です。