溶媒:
*溶質を溶かす物質。
*通常、溶質よりも大量に存在します。
*溶液の状態を決定します(たとえば、水は液体溶媒であり、水溶液を作成します)。
溶質:
*溶媒に溶解する物質。
*通常、溶媒よりも少ない量で存在します。
*固体、液体、またはガスにすることができます。
関係:
* 溶解: 溶媒は溶質粒子を囲み、それらをバラバラにし、溶媒全体に分散させます。
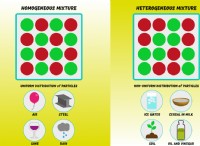
* 均一な混合物: 結果は均質な混合物であり、溶質と溶媒が均等に分布し、互いに区別できないことを意味します。
* 分子間力: 溶媒分子と溶質分子間の相互作用により、溶質がどれだけうまく溶解するかが決まります。同様の極性(たとえば、水は極性、砂糖は極性)が一般的に溶解度が向上します。
* 濃度: 特定の量の溶媒に溶解した溶質の量は、濃度と呼ばれます。
例:
* 塩水: 水は溶媒であり、塩は溶質です。塩が水に溶けると、水分子が塩イオンを囲み、それらをバラバラにし、水全体に分散させます。
キーポイント:
*溶媒は、溶解する物質です。
*溶質は溶解する物質です。
*結果の混合物は均一な溶液です。
より多くの例が欲しいのか、溶解度に影響を与える要因をより深く掘り下げたい場合はお知らせください!