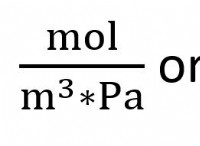その理由は次のとおりです。
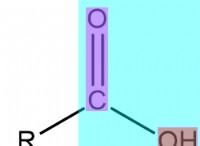
* ルイス構造: 炭酸イオンのルイス構造は、3つの酸素原子に結合した中心に炭素を示しています。
* 共鳴: 炭酸イオンは共鳴を示します。つまり、二重結合は炭素と3つの酸素原子のいずれかの間に描画できます。これは、各酸素原子に二重結合と単一の結合を描くことによって表されます。これは、電子の非局在化を示す線系です。
* 非局在電子: 二重結合は、実際には3つの炭素酸素結合すべてにわたって非局在化されています。これは、電子がそれらの間で均等に共有され、それらがすべて長さと強度がすべて同等になることを意味します。
したがって、ルイス構造は一度に1つの二重結合のみを示していますが、真の表現には、部分的な二重結合特性を持つ3つの等価結合が含まれます。