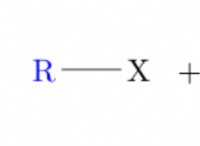これが故障です:
* 原子: 分子の基本的な構成要素。
* 債券: 原子を分子にまとめる力。
* 結合角: 共通原子を共有する2つの隣接する結合間の角度。
結合角に影響する要因:
* ハイブリダイゼーション: 原子軌道が混ざり合って新しいハイブリッド軌道を形成する方法は、分子の形状、したがって結合角に影響します。たとえば、SP3のハイブリダイゼーションは通常、109.5°前後の結合角で四面体の形状につながります。
* 孤立ペア: 中央原子に電子の孤立ペアが存在すると、結合角が結合角を減らすことができます。
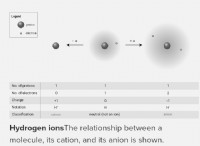
* 電気陰性度: 結合に関与する原子の電気陰性度も結合角に影響を与える可能性があります。
例:
水分子(H2O)では、酸素原子は水素原子と2つの結合を形成します。これら2つの結合間の結合角は約104.5°です。この角度は、酸素原子に2つの孤立した電子の存在が存在するため、理想的な四面体角(109.5°)よりわずかに少ないです。
結合角度を理解することは、化学において重要な役割を果たしているため、次のことを重要な役割を果たすため、化学には重要です。
*分子形状
*分子極性
*化学反応性
*物理的特性(たとえば、融点、沸点)