その理由は次のとおりです。
* 窒素(n) 5つの価電子があります。
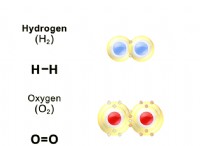
* 酸素(O) 6つの価電子があります。
安定したイオンを形成するには、電子を獲得または失う必要はありません。ただし、A 共有結合を形成する可能性が高くなります 彼らが電子を共有する場所。
一般的な非含有イオン:
* no⁺(ニトロシルカチオン): このイオンには+1電荷があり、noから電子の損失によって形成されます。
* no₂⁻(亜硝酸アニオン): このイオンには-1電荷があり、1つの窒素原子と2つの酸素原子が含まれています。
* no₃⁻(硝酸アニオン): このイオンには-1電荷があり、1つの窒素原子と3つの酸素原子が含まれています。
したがって、非含有イオンの電荷を決定するには、参照している分子を指定する必要があります。