カタラーゼに対する硫酸の阻害効果:構造と化学の見方
カタラーゼは、過酸化水素(h₂o₂)を水(h₂o)と酸素(o₂)に分解する酵素です。これは、反応性酸素種の損傷効果から細胞を保護するために重要です。硫酸(H₂SO₄)はカタラーゼ活性を阻害します。これがどのように機能するかを示します。
1。酵素構造とメカニズム:
*カタラーゼは、4つの同一サブユニットを持つ四量体タンパク質です。各サブユニットには、その中心に鉄の原子を備えたポルフィリンリング複合体であるヘムグループが含まれています。
*ヘム群はカタラーゼの活性部位であり、酵素の触媒活性の原因です。
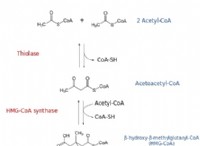
*反応メカニズムには、次の手順が含まれます。
*h₂o₂はヘム鉄に結合します。
*ヘム群の鉄原子は、h₂o₂を酸化してI中間化合物を形成します。
*化合物Iは、H₂O₂の別の分子と反応して水と酸素を生成し、活性部位を再生します。
2。硫酸の衝撃:
*硫酸は強酸であり、陽子を容易に寄付することを意味します(H⁺)。
*硫酸が反応混合物に添加されると、酵素の構造と機能をいくつかの方法で破壊する可能性があります。
* アクティブサイトのプロトン化: 硫酸のプロトンは、ヘム群の鉄原子に結合し、電子状態を変えます。これは、過酸化水素を結合して活性化するヘムの能力を破壊し、触媒サイクルを効果的にブロックすることができます。
* 変性: 硫酸は、タンパク質の三次および四級構造を破壊する可能性があります。これは、酸のプロトンがタンパク質の3次元形状を形成するアミノ酸側鎖と相互作用できるためです。 結果として生じる変性は、酵素の展開につながり、活性部位を露出させ、最終的にそれを不活性化します。
* pH効果: 硫酸の強い酸性度は、反応混合物のpHを劇的に低下させます。カタラーゼは活性に最適なpH範囲を持ち、極端なpH値は酵素に不可逆的な損傷を引き起こす可能性があり、それを非アクティブにします。
3。概要:
カタラーゼに対する硫酸の阻害効果は、その酸性の性質に由来します。活性部位をプロトン化し、酵素の構造を破壊し、pHを下げることができ、すべてカタラーゼの不活性化に寄与します。これは、過酸化水素の蓄積につながり、細胞を損傷する可能性があります。
重要な注意: 阻害の正確なメカニズムは、硫酸の濃度やその他の要因によって異なる場合があります。ただし、原理は同じままです。硫酸はカタラーゼの構造と機能を破壊し、最終的にその活性を阻害します。