その理由は次のとおりです。
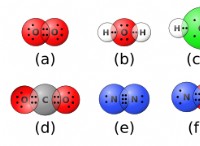
* 水素(H) 周期表のグループ1にあります。つまり、1原子価電子を持ち、+1カチオン(H⁺)を形成するために失う傾向があります。
* 塩素(cl) 周期表のグループ17にあります。つまり、7つの原子価電子を持ち、1電子を獲得して-1アニオン(Cl⁻)を形成する傾向があります。
ニュートラル化合物を形成するには、料金のバランスを取る必要があります。 水素は1つの電子を失い、塩素は1つの電子を獲得するため、それらは1:1の比で結合し、式 hcl になります 。
重要な注意: HCLは技術的にはイオン化合物ですが、強酸でもあります。水溶液では、完全に分離してh⁺イオンに分離します。