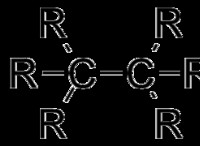
飽和結合
* 定義: 飽和結合は、原子の周りのすべての結合位置が単一結合で満たされている化学結合を指します。これは、二重または三重の結合が存在しないことを意味します。
* 重要な特性:
* 単一結合: 単一の共有結合のみが存在します。
* 最大水素原子: 飽和化合物には、保持できる水素原子の最大数が含まれています。
* 安定性: 飽和結合は、一般に、電子の偶数分布のため、不飽和結合よりも安定しています。
飽和結合を持つ化合物
* アルカン: これらは、単一の結合しかない炭化水素(炭素と水素で作られています)です。例:メタン(CH4)、エタン(C2H6)、プロパン(C3H8)。
* cycloalkanes: 単一の結合のみの周期的な炭化水素。例:シクロプロパン(C3H6)、シクロヘキサン(C6H12)。
* 飽和脂肪酸: 一端にカルボン酸基(-COOH)を備えた炭化水素の長い鎖。 これらは脂肪と油に見られます。 例:パルミチン酸、ステアリン酸。
* 飽和アルコール: すべての炭素間に単一結合を持つアルコール。例:メタノール(CH3OH)、エタノール(C2H5OH)。
飽和結合の例:
* メタン(CH4): 炭素原子の周りの4つの結合はすべて、水素原子への単一結合です。
* エタン(C2H6): 各炭素原子は、3つの水素原子と、単一結合を持つ他の炭素原子に結合されます。
重要な注意:
* 不飽和債券: 二重結合または三重結合を持つ化合物は不飽和と見なされます。 例には、アルケン(二重結合付き)、アルキン(トリプル結合を含む)、不飽和脂肪酸が含まれます。
飽和結合を含む特定の種類の化合物や反応についてもっと知りたい場合はお知らせください!