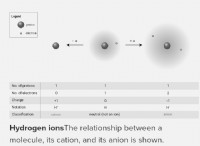
その理由は次のとおりです。
* 原子価シェルの電子は化学結合に関与するものです。 彼らは核から最も遠いものであり、それに対する最も弱い魅力を経験します。これにより、他の原子と相互作用する可能性が高くなります。
* 原子電子の数が原子の反応性を決定します。 原子は、通常の価数シェル(2つの電子を持つ完全なシェルを持つ水素とヘリウムを除き、8電子を除く)で、安定した構成を実現するために電子を獲得、失い、または共有する傾向があります。
* 原子が形成できる結合のタイプを決定する原子価電子の配置は たとえば、1つまたは2つの原子価電子を持つ原子はそれらを失い、イオン結合を形成する傾向がありますが、4つ以上の価電子を持つ原子は電子を共有し、共有結合を形成する傾向があります。
要約すると、原子が他の原子、したがってその化学的特性とどのように相互作用するかを決定する上で、原子価シェルは重要な役割を果たします。