出発点:
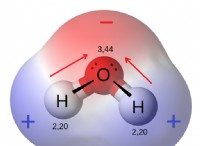
*硫酸銅(Cuso₄)溶液は、水和銅(II)イオン(Cu²⁺(aq))の存在のため青色です。
電解:
* カソード(負の電極): 銅(II)イオン(Cu²⁺)は銅金属(Cu)に還元されます。
cu²⁺(aq) +2e⁻→cu(s)
* アノード(正の電極): 水分子は、酸素ガス(O₂)および水素イオン(H⁺)に酸化されます。
2h₂o(l)→o₂(g) +4h⁺(aq) +4e⁻
色の変化:
* 青から無色: カソードで銅イオンが減少し、銅金属として堆積すると、溶液中のcu²⁺イオンの濃度が減少します。これにより、青色の強度が低下します。
* さらなる変化の可能性: 電気分解が継続すると、ほとんどの銅イオンが除去されるため、溶液は最終的にほとんど無色になる可能性があります。ただし、陽極でのH×イオンの形成により、溶液は依然として酸性になります。
全体的な反応:
硫酸銅溶液の電気分解中の全体的な反応は、次のように要約できます。
2cuso₄(aq) +2h₂o(l)→2cu(s) +o₂(g) +2h₂so₄(aq)
重要な注意: 電気分解中の色の変化は、溶液中に発生する化学変化の視覚的指標です。これは、銅イオンの減少と溶液中の濃度の枯渇の結果です。