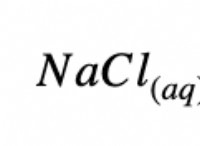モラリティの理解
* モラリティ(M) 濃度の尺度、特に1リットルの溶液に溶解した溶質のモル数です。
* ほくろ 個々のアイテムをカウントするなど、物質の量の単位です。
* 溶質 溶解する物質(塩、砂糖など)です。
* 溶媒 溶解する物質(たとえば、水)です。
同じ臼歯の2つの溶液を作成する手順
1。溶質と望ましいモル濃度を選択します:
*溶解したい物質(溶質)を決定します。
*目的のモル濃度(0.5 m、1.0 mなど)を選択します。
2。必要な溶質の質量を計算します:
* 式: 質量(g)=モル濃度(m)×体積(L)×モル質量(g/mol)
* モル質量: 周期表または化学的参照で溶質のモル質量を調べます。
3。溶質を既知の溶媒で溶解する:
*計算された溶質の質量を正確に計量します。
*溶質を、目的の体積の体積フラスコに追加します(例:100 mL、250 mL、1 Lなど)。
*ゆっくりと溶媒(通常は水)をフラスコに加え、ゆっくりと渦巻いて溶質を完全に溶かします。
*フラスコがほぼいっぱいになったら、メニスカス(液体の曲線)がフラスコのキャリブレーションマークに達するまで、溶媒の最終部分を慎重に追加します。
4。 2番目のソリューションで繰り返します:
* 2番目のソリューションを作成するために、同じ溶質、望ましいモル濃度、および同じ手順を使用します。
例:塩化ナトリウム(NaCl)の2つの0.5 m溶液を作る
1。溶質: NaCl
* 望ましいモル濃度: 0.5 m
2。質量を計算します:
* NaClのモル質量: 58.44 g/mol
* ボリューム: 各溶液の250 mL(0.25 L)を作成したいと仮定しましょう。
* 質量(g): 0.5 m×0.25 l×58.44 g/mol =7.31 g
3。溶解:
* 7.31 gのNaClを計量します。
* 250 mlの体積フラスコに追加します。
*ゆっくりと水を加え、渦巻いてNaClを溶かします。
*フラスコを250 mlのマークに水で満たします。
4。繰り返し: 同じ手順に従って、0.5 m NaClの2番目の250 mL溶液を作成します。
重要な考慮事項:
* 精度: 分析バランスを使用して、溶質を正確に計量します。
* 体積フラスコ: 体積フラスコは、正確な体積測定用に設計されています。
* 温度: 臼歯は温度依存です。さまざまな温度でソリューションが使用される場合、潜在的な体積の変化を因数分解します。
* 安全性: 化学物質を扱うときは、常に適切な安全装置(手袋、ゴーグル)を着用してください。