1。イオンを特定します:
* マグネシウム(mg) 周期表のグループ2の金属です。 +2電荷で陽イオンを形成するために2つの電子を失う傾向があります:mg²⁺
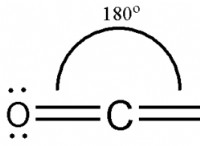
* 酸素(O) 周期表のグループ16の非金属です。 -2電荷でアニオンを形成するために2つの電子を獲得する傾向があります:o²⁻
2。料金のバランス:
*マグネシウムイオン(mg²⁺)と酸化物イオン(o²⁻)の電荷は、すでに等しく反対です。 これは、ニュートラル化合物を作成するには、各イオンの1つが必要です。
3。式を書きます:
*酸化マグネシウムの式は mgo です 。
重要な原則: 目標は、イオン化合物の中性全体の電荷を達成することです。 陽イオンとアニオンの電荷はバランスを取る必要があります。