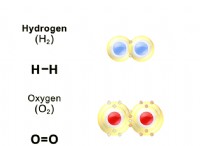
* 電気陰性度: 非金属は、金属よりも電気陰性度が高い。これは、彼らが電子のより強い魅力を持っていることを意味します。
* オクテットルール: 非金属は、8つの電子の完全な外殻を達成するために電子を獲得する傾向があります(オクテットルール)。これにより、貴族と同様の安定した電子構成が得られます。
例:
ナトリウム(Na)と塩素(Cl)の間の反応を考えてみましょう。
*ナトリウム(NA)は金属であり、その外側の殻に1つの電子があります。この電子を容易に失い、積極的に帯電したイオン(Na+)になります。
*塩素(Cl)は、外殻に7つの電子を備えた非金属です。 1つの電子を獲得して、負に帯電したイオン(CL-)になります。
得られたイオン化合物である塩化ナトリウム(NaCl)は、正に帯電したナトリウムイオンと負に帯電した塩化物イオンとの間の静電引力によって形成されます。
要約: 非金属は電子受容体であり、安定した電子構成を実現するために電子を獲得し、負に帯電したイオン(アニオン)を形成します。